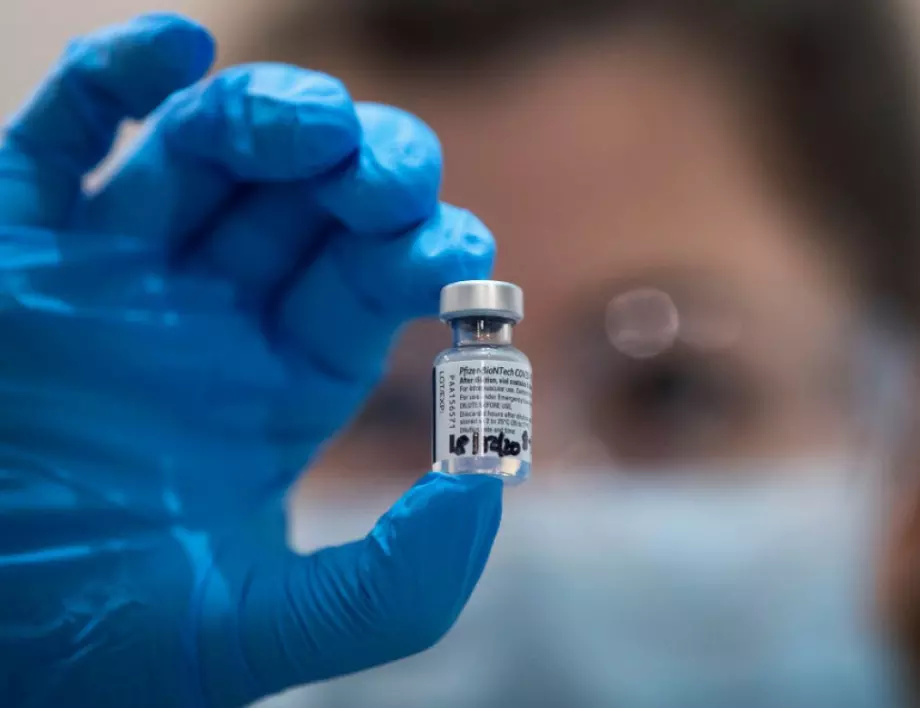
Темата с ползите и рисковете около ваксината срещу COVID-19 на Pfizer/BioNTech предизвика разнопосочни коментари. Вече излезе и предварителният доклад за свойствата на въпросната ваксина.
Още: Как да се пазим от кърлежи и комари? Съветите от проф. Кантарджиев
Още: Бургас с детска болница до края на годината, но национална няма
От него става ясно, че при 38 000 доброволци, участвали в третата фаза на клиничните проучвания, има 6 починали – 2 от тях са получили ваксина, а 4 от починалите са в плацебо групата. Случаите на двамата починали, които са получили ваксина, са следните: един участник с атеросклероза и затлъстяване е починал три дни след първата доза от лекарството, а друг участник е претърпял сърдечен удар 60 дни след поставяне на втората доза.
От данните, които Pfizer/BioNTech представи, се вижда, че рисковете при двете групи – тези, действително получили ваксина, и тази с плацебо, са сходни. Хората в групата на ваксинираните са били застрашени от 0.5% риск от по-тежки странични ефекти, докато този риск при плацебо е бил 0.4%. Най-много оплаквания има от сърдечни проблеми (0.1% риск и в двете групи), нервни проблеми (0.1% и при двете групи), инфекции и инвазии (0.1% и при двете групи).
Днес се очаква група от експерти да разгледа доклада на Американската агенция по храните и лекарствата (FDA), като по-рано самата Агенция публикува документа на производителя на ваксината Pfizer/BioNTech.
Още: Тежкият път да одобрят дете за лечение в чужбина и колко помага държавата
Още: Това ще влоши качеството на услугата: Болниците недоволни от намалената таксата за престой
Независими и обективни новини - Actualno.com ги представя и във Viber! Последвайте ни тук!
Още: Съмнения за зараза в Банско: Проверяват водата
Още: Детска ортопедия и вродени малформации – безплатни консултации с д-р Чабукоглу
Още: Д-р Татяна Мороховец: Как да противодействаме на стомашните киселини?
Ползи от ваксината, описани в доклада пред FDA:
- Между приема на първата и втората доза рискът от заразяване с COVID-19 намалява;
- Рискът от заразяване с COVID-19 пада най-малко 7 дни след поставянето на втората доза;
- Рисковете от тежко протичане на заболяването намаляват по всяко време след поставянето на първата доза от ваксината.
Рискове от ваксината, описани в доклада пред FDA:
- Не е ясна ефективността на ваксината след приема на втората доза и изтичането на двумесечния период от това. Причината за тази неизвестност е свързана с клиничното проучване, продължило 2 месеца;
- Не става ясно как ваксината ще покаже ефективност при асимптоматично заболяване, тъй като към момента данните са твърде ограничени, за да се направят изводи дали антителата са имунен отговор, предизвикан от ваксината, или са реакция на самата зараза.
- По отношение на дългосрочните ефекти от COVID-19, засягащи определен органи, не е ясно каква е ефективността на ваксината, за да ги предпази от увреждане.
- Не е ясно доколко ваксината участва в намаляването на смъртността вследствие на заболяването. За да се изследва този показател, е необходимо да се провери действието на ваксината върху много по-голям брой хора с висок риск от COVID-19. Въпреки това други ваксини (например тази срещу грип), които са ефикасни срещу болестта, предотвратяват и свързаната с болестта смъртност.
- Остава неясна ефективността на ваксината срещу разпространението на COVID-19 – няма достатъчно данни, за да се установи ефективността срещу разпространение на вируса от индивиди, които са заразени въпреки ваксинацията.
Рискове от ваксината, които към момента са познати:
- От доклада става ясно, че ваксината може да предизвика реакция, която продължава известен брой дни. Тази реакция (или реакции) могат да бъдат леки и/или умерени.
- Най-известните проявени странични ефекти са: реакция на мястото на инфекцията (84.1%), умора (62.9%), главоболие (55.1%), мускулни болки (38.3%), изтръпвания (31.9%), болки в ставите (23.6%), температура (14.2%);
- Сериозни неблагоприятни реакции са документирани при 0.0 – 4.6% от участниците. Те са били по-чести след приемане на доза 2 и то при хората под 55 години (4.6%) в сравнение с по- възрастните от 55 г. (под 2.8%).
- Има информация, че ваксината може да е свързана с някои случаи на лимфаденопатия (подуване на лимфните възли), която се среща и при прилагането на други ваксини, както и при обикновена настинка.
- Отбелязани са много редки случаи на сериозни неблагоприятни събития (под 1%), но те са с една и съща честота както във ваксинираната група, така и в общото население. По-конкретно става дума за нараняване на рамо (1 случай), вентрикуларна аритмия (1 случай на пациент със сърдечно заболяване) и лимфаденопатия.
Рискове, произтичащи от липсата на данни:
- В доклада е посочено, че не е известно доколко ваксината е безопасна при деца под 16-годишна възраст, при бременни жени и кърмачки, както и при имунокомпрометирани лица. Все пак производителят посочва, че случаите на неблагоприятни реакции са много редки или изискват по-дълъг период, за да бъдат регистрирани;
- По време на третата фаза от проучванията, във ваксинираната група са регистрирани по-голям брой случаи на апендицит в сравнение с плацебо групата, но броят им съответства на съотношението в общото население и засега не се открива причинно-следствена връзка между ваксината и случаите на апендицит;
- Докладвани са четири случая на т. нар. 'парализа на Бел' (парализа или слабост на мускулите на едната половина от лицето) в сравнение с 0 случаи в плацебо групата. Въпросните 4 случая обаче не са по-висока честота в сравнение със стандартната в населението при съответствие на възрастовите групи;
- Придобитите към момента данни не показват риск от усложнения на заболяването COVID-19 заради ваксината.
С подробностите от доклада (на английски език) за ваксината на Pfizer/BioNTech може да се запознаете тук.